【www.zhangdahai.com--其他范文】
张丽芳,武 欢,张 乐
(沈阳理工大学环境与化学工程学院,沈阳 110159)
矿业、冶金、制革、电镀等行业重金属废水排放不断增长,生态环境面临重金属污染风险日益加大。
废水中的重金属离子无法降解,同时还可在食物链中富集,甚至在人体内蓄积,危害人类健康[1-2]。
传统重金属离子处理方法包括化学沉淀、吸附、离子交换、电化学法及膜交换等[3-4]。吸附法因其高效、价廉以及操作简便等特点,在重金属废水治理中得到广泛关注[5-6]。
壳聚糖为绿色环保的天然高分子材料,来源广泛,是一种良好的重金属吸附材料,其分子链上存在大量的氨基(—NH2)及羟基(—OH)等活性官能团,可作为吸附重金属离子的活性位点[7-8]。壳聚糖虽然具有吸附性,但其对重金属离子吸附能力有限,对壳聚糖进行适当改性,提高其吸附性能成为当下研究热点。
目前,壳聚糖物理改性一般是通过制备微球、薄膜等方法改变壳聚糖的物理特性;
化学改性是通过与其他物质反应而改变其物理及化学性能,常用的化学改性方法有季铵盐化、交联化、烷基化等[9-11]。
冯辉霞等[12]用硅藻土改性壳聚糖,制备了硅藻土复合磁性壳聚糖,与未改性壳聚糖相比,其对Cr(Ⅵ)的吸附效果显著提升。
赵娜等[13]采用滴加成球方法制备了壳聚糖交联螺旋藻小球,将其用于吸附Cr(Ⅵ),实验结果表明吸附效果良好。
王丽丽等[14]利用聚乙烯亚胺对壳聚糖进行接枝改性,并用于多种金属离子的吸附,研究结果表明其对Cu(Ⅱ)的吸附效果最好,吸附量可达53.76mg/g。
高爱莎等[8]利用天冬氨酸通过酯化反应改性壳聚糖,制备的改性磁性壳聚糖对Cd(Ⅱ)具有较好的去除效果。
为提高壳聚糖的吸附性能,本文采用物理化学改性,利用超声协同Fe3O4改性壳聚糖。
本文创新之处在于壳聚糖无需纳米化,也无需步骤复杂的接枝或酯化等化学改性,仅需超声破碎后一步交联即可,过程简单,易于控制。
首先对壳聚糖进行超声破碎,然后以戊二醛为交联剂,将Fe3O4负载到壳聚糖上;
采用扫描电镜、红外光谱以及X射线衍射等对改性壳聚糖表征分析;
考察Fe3O4用量、交联剂用量等因素对Fe3O4改性壳聚糖吸附能力的影响。
1.1 实验主要试剂与原料
氢氧化钠、冰乙酸、硫酸、无水乙醇、二苯碳酰二肼、重铬酸钾、三氯化铁(FeCl3·6H2O)、七水合硫酸亚铁(FeSO4·7H2O),均为分析纯,国药集团化学试剂有限公司;
戊二醛,分析纯,天津市大茂化学试剂厂。
壳聚糖,商品级(脱乙酰度≥90%),桓台县金湖甲壳制品有限公司。
1.2 实验方法
1.2.1 Fe3O4改性壳聚糖的制备
分别将浓度为0.5mol/L 的FeSO4·7H2O 和0.5mol/L 的FeCl3·6H2O 溶液,按Fe2+与Fe3+物质的量比为1∶2 混合,迅速加入氢氧化钠溶液,调节pH 值为13 ~14,密封;
在130r/min、75℃水浴振荡器(SHA-C 型,常州国华电器有限公司)中振荡反应1h,然后移入75℃烘箱(101-2AB 型,天津市泰斯特仪器有限公司) 内晶化1h;
在8000r/min下离心洗涤至中性,无水乙醇脱水,得Fe3O4粉末。
将0.4g 壳聚糖溶解于2%的乙酸溶液中,在超声波细胞粉碎机(Scientz-ⅡD,宁波新芝生物科技股份有限公司)中破碎一定时间,移取一定体积的2.5%戊二醛溶液,加入一定质量的Fe3O4粉末,充分混匀,静置2h;
将混合液用注射器缓慢滴入到1mol/L 的氢氧化钠溶液中,静置20min,用去离子水多次洗涤直至中性,烘干,得Fe3O4改性壳聚糖备用。
1.2.2 改性壳聚糖对Cr(VI)的吸附
将50mg Fe3O4改性壳聚糖置于50mL、浓度和pH 值已知的Cr(VI)溶液中,在温度为30℃(另有说明除外)、转速为130r/min 的恒温振荡器中吸附。
待吸附达到平衡后,过滤,上清液中Cr(VI)的浓度测定采用二苯碳酰二肼分光光度法[15],重复测定三次取均值。
溶液中Cr(VI)的去除率和吸附量的计算公式如下。

式中:r为去除率,%;
C0和Ce分别为Cr(VI)的初始浓度和吸附平衡时的浓度,mg/L;
qe为平衡吸附量,mg/g;
V为溶液体积,L;
m为改性壳聚糖的质量,g。
1.2.3 材料的表征
采用美国赛默飞世尔科技公司Nicolet6700型傅里叶变换红外光谱仪(FT-IR)对Fe3O4及改性前后的壳聚糖结构进行表征,溴化钾压片制样,测量波数范围为4000 ~500cm-1,扫描32 次;
采用日立S-3400N 型扫描电镜(SEM)测定Fe3O4及改性前后的壳聚糖形貌;
采用德国布鲁克D8 Advance X 射线衍射仪(XRD)进行物相分析,衍射角扫描范围为5 ~90°;
采用麦克默瑞提克仪器有限公司ASAP 2460 多站扩展式全自动快速比表面与孔隙度分析仪进行BET 比表面积及孔径的测定,样品经真空干燥后,进行N2吸附-脱附;
采用上海中晨JS94H2微电泳仪测定改性壳聚糖的Zeta 电位。
2.1 Fe3O4 改性壳聚糖的表征
2.1.1 FT-IR 分析
对壳聚糖原样、Fe3O4及Fe3O4改性壳聚糖样品分别进行红外光谱扫描分析,结果如图1所示。
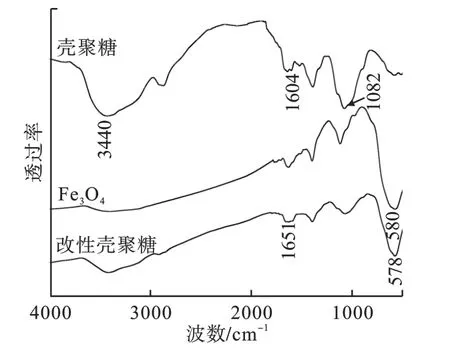
图1 FT-IR 图
图1中壳聚糖的谱线在波数3440cm-1附近为O—H 和N—H 的伸缩振动峰,1604cm-1处为—NH2中N—H 的弯曲振动峰,1082cm-1处为C—OH 的伸缩振动峰[16-18];
图1中Fe3O4的谱线在580cm-1附近为Fe—O 的振动峰[18-19];
图1中改性壳聚糖的谱线在1651cm-1处可见C=N的伸缩振动峰,在578cm-1处可见Fe3O4的Fe—O特征峰,说明壳聚糖分子上的—NH2与戊二醛分子上的—CHO 发生交联反应,形成席夫碱,同时Fe3O4颗粒负载到壳聚糖表面。
2.1.2 SEM 分析
分别对壳聚糖、Fe3O4、戊二醛交联壳聚糖以及Fe3O4改性壳聚糖样品进行SEM 表征,结果如图2所示。

图2 SEM 图
由图2a 可见,壳聚糖表面无颗粒状物质,呈片层状光滑结构;
由图2b 可见,Fe3O4为大小不一的颗粒状结构,对Fe3O4颗粒进行BET 测定,其BET 比表面积为70. 57m2/g、平均孔径为11.33nm、孔容为0.19996cm3/g;
由图2c 可见,戊二醛交联后壳聚糖(无Fe3O4)表面不再光滑,结构发生变化,呈现不规则隆起;
由图2d 可见,壳聚糖经Fe3O4改性后,其表面更多隆起、更为粗糙,且布满大量颗粒状Fe3O4。
2.1.3 XRD 分析
改性前后的壳聚糖及Fe3O4的XRD 分析结果见图3所示。

图3 XRD 图
由图3可见,改性前壳聚糖的XRD 谱线在衍射角为20°处有一显著锐利的单衍射峰。
这是由于壳聚糖分子含有丰富的—NH2和—OH 等官能团,易形成氢键,在氢键作用下壳聚糖形成规则有序的大分子结构,故出现显著的结晶衍射峰。Fe3O4的XRD 谱线有6 个特征衍射峰,分别对应Fe3O4的(220)、(311)、(400)、(422)、(511)、(440)晶面,谱线上未见杂质峰。
改性后壳聚糖的XRD 谱线在20°处的特征衍射峰峰强显著减弱,这是由于戊二醛与壳聚糖的交联作用破坏了壳聚糖内部广泛存在的氢键,降低了壳聚糖的结晶度。与Fe3O4的谱线对比,改性壳聚糖的谱线在相同位置处出现相同的衍射峰,表明Fe3O4成功负载到壳聚糖上。
2.2 改性条件对去除率的影响
2.2.1 Fe3O4用量的影响
戊二醛用量取为20mL/g,超声破碎时间为4min,在不同的Fe3O4用量(0 ~0.625g/g)下制备改性壳聚糖,并将其用于Cr(VI)的吸附,以未改性壳聚糖、Fe3O4做对照实验,结果如图4所示。

图4 Fe3O4 用量对去除率的影响
由图4可知,未改性壳聚糖和Fe3O4对Cr(VI) 的去除率较低, 分别为34. 45% 和26.98%。
未采用Fe3O4改性的戊二醛交联壳聚糖对Cr(VI)的去除率为37.55%,表明壳聚糖经戊二醛交联后,对吸附有一定的促进作用;
壳聚糖经Fe3O4改性后,对Cr(VI)的去除率均高于壳聚糖或Fe3O4。
当Fe3O4用量由0.0125g/g 升高到0.25g/g,吸附剂表面积有所增加,改性壳聚糖对Cr(VI)的去除率也相应升高;
Fe3O4添加量达到0.25g/g 时,去除率最大,为49.3%;
此后继续增加Fe3O4用量,过多Fe3O4阻碍壳聚糖吸附位点与Cr(VI)接触,去除率开始下降。
适宜的Fe3O4用量为0.25g/g。
2.2.2 戊二醛用量的影响
Fe3O4用量取为0. 25g/g,超声破碎时间为4min,在不同戊二醛用量(7.5 ~35mL/g)下制备改性壳聚糖,并将其用于Cr(VI)的吸附,结果如图5所示。
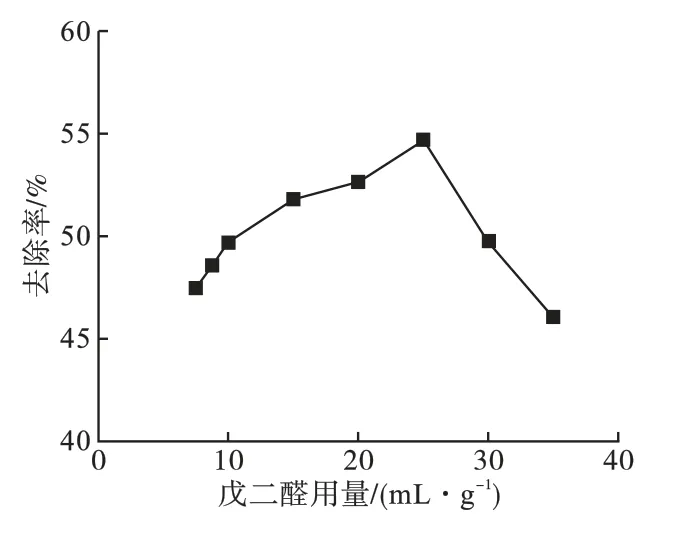
图5 戊二醛用量对去除率的影响
由图5可知,交联剂戊二醛的投加量对改性壳聚糖吸附Cr(VI)有显著影响。
当戊二醛用量由7.5mL/g 增加到25mL/g 时,改性壳聚糖对Cr(VI)的去除率明显升高,用量为25mL/g 时去除效果最优,去除率为54.69%;
在酸性溶液中,经戊二醛交联后的壳聚糖溶解性下降,结构稳定性得到提高,且壳聚糖经戊二醛交联后改变了原有结构,破坏了内部氢键,释放了部分活性位点,更有利于对Cr(VI)的吸附。
当戊二醛的用量大于25mL/g 时,改性壳聚糖对Cr(VI)的吸附去除作用迅速降低;
这是因为壳聚糖分子中的—NH2和戊二醛分子中的—CHO 发生席夫碱反应,生成了—C=N—基团[20],在改性过程中,壳聚糖用量不变,戊二醛用量过多时,因席夫碱反应消耗了壳聚糖上大量的—NH2,削弱了改性壳聚糖对Cr(VI)的吸附。
故适宜的戊二醛用量为25mL/g。
2.2.3 超声破碎时间的影响
戊二醛用量取为25mL/g,Fe3O4用量取为0.25g/g,在不同超声破碎时间(0 ~30min)下制备改性壳聚糖,并用于吸附Cr(VI),结果如图6所示。
由图6可知,随着超声破碎时间增加,改性壳聚糖对Cr(VI)的去除率先增大后减小,超声破碎时间为5min 时,Fe3O4改性壳聚糖对Cr(VI)离子的去除率最大,为55.15%。
这是由于壳聚糖经过适宜的超声破碎增加了吸附质和吸附剂接触面积,有利于对Cr(VI)吸附;
壳聚糖超声破碎时间过长,其粒径变小,当戊二醛用量一定时,交联度下降,影响吸附效果。
适宜的超声破碎时间为5min。
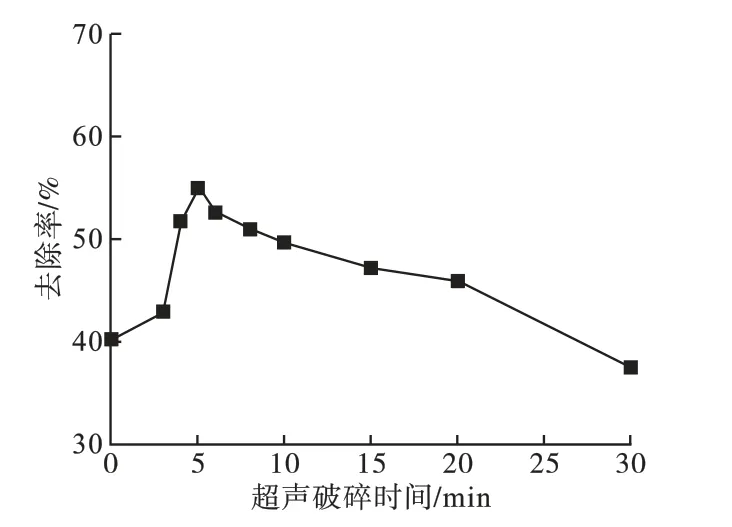
图6 超声破碎时间对去除率的影响
2.3 吸附条件对去除率的影响
2.3.1 pH 的影响
调节Cr(VI)溶液初始pH 值为1.5 ~8,在吸附温度为30℃、吸附时间为240min、Cr(VI)溶液初始浓度为20mg/L 的条件下,测得Fe3O4改性壳聚糖对Cr(VI)的去除率,如图7所示。

图7 pH 对去除率的影响
由图7可知,在pH 值由1.5 升至4 时,Fe3O4改性壳聚糖对Cr(VI)的去除率缓慢升高,初始pH值为4 时,去除率升至最大,为57.37%;
当pH 值超过4 时,去除率快速降低。
对Fe3O4改性壳聚糖的Zeta 电位进行测定,结果如图8所示。
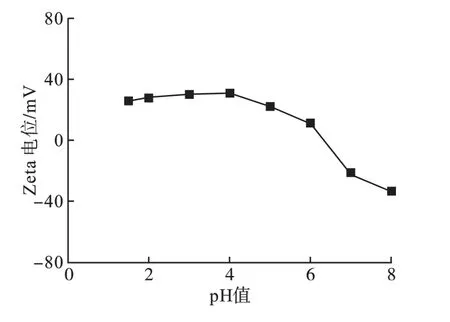
图8 Fe3O4 改性壳聚糖的Zeta 电位
由图8可知,Fe3O4改性壳聚糖的零点电位在pH 值约为6.3 左右;
当溶液pH 值低于6.3 时,改性壳聚糖的Zeta 电位为正值;
pH 值超过6.3 时,Zeta 电位为负值。
Cr(VI)因溶液pH 的不同而呈现不同的存在形式,在酸性溶液中主要为HCrO4-与Cr2O27-阴离子,碱性溶液中主要为CrO24-。
在较低pH 下,改性壳聚糖游离的—NH2被电离为NH3+,其表面带正电荷,易与Cr(VI)产生静电吸附。
pH 值为1.5 ~6.3 时,改性壳聚糖表面带正电荷,且pH 值为4 时,Zeta 电位绝对值最大,此时改性壳聚糖对Cr(VI)的吸附效果最好。
当pH 值大于6.3 时,改性壳聚糖表面游离—NH2电离能力减弱,其表面带负电,且pH 值越大,电负性越强,因而在高pH 值条件下,不利于改性壳聚糖对Cr(VI)的吸附。
故适宜的pH 值为4。
2.3.2 吸附温度的影响
改变吸附温度(20 ~60℃),在pH 值为4、吸附时间为240min、Cr(VI)溶液初始浓度为20mg/L 的条件下,测得Fe3O4改性壳聚糖对Cr(VI)的去除率,如图9所示。
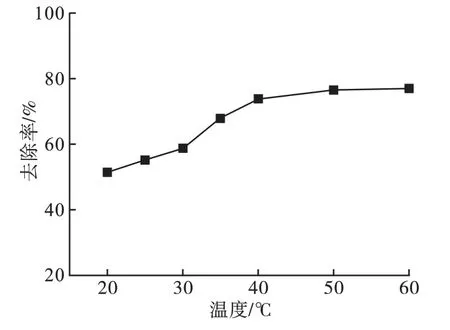
图9 吸附温度对去除率的影响
由图9可知,吸附温度由20℃升高至40℃时,改性壳聚糖对Cr(VI)的去除率明显提高,由51.5%提高至73.84%,温度超过40℃后,去除率增加变得平缓。
说明吸附温度在20 ~40℃范围内,升高温度对改性壳聚糖的吸附效果有明显促进作用。
2.3.3 吸附时间的影响
在pH 值为4、吸附温度为30℃、Cr(VI)初始浓度为20mg/L 时,改变吸附时间(5 ~270min),测得Fe3O4改性壳聚糖对Cr(VI)的吸附量,如图10所示。
由图10 可知,在初始的60min 范围内,随着吸附时间增加,改性壳聚糖对Cr(VI)的吸附量迅速升高,吸附时间由60min 增至240min 时,吸附量增速变缓,约在240min 时建立吸附平衡。
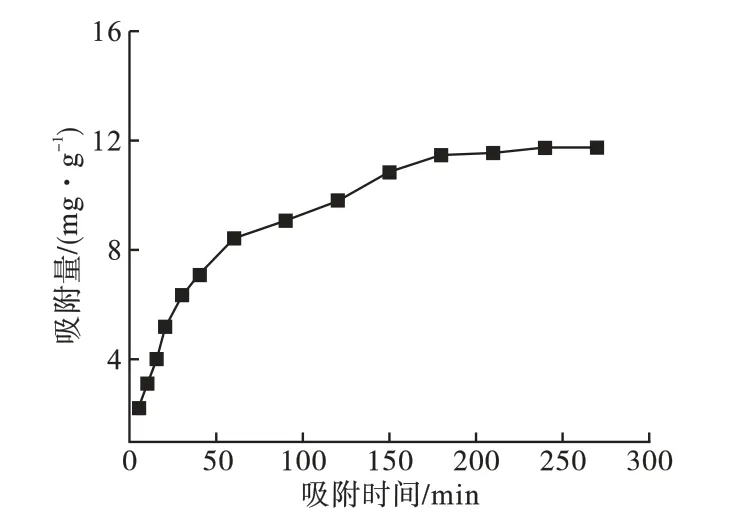
图10 吸附时间对吸附量的影响
2.3.4 初始浓度的影响
在pH 值为4、吸附时间为240min、温度为30℃时,改变Cr(VI)溶液初始浓度C0(10 ~100mg/L),测得Fe3O4改性壳聚糖对Cr(VI)的平衡吸附量qe,如图11 所示。

图11 初始浓度对平衡吸附量的影响
由图11 可知,初始浓度由10mg/L 升至80mg/L时,改性壳聚糖对Cr(VI)离子的平衡吸附量快速增加;
初始浓度为80mg/L 时,平衡吸附量达到47.07mg/g;
之后继续升高Cr(VI)初始浓度,平衡吸附量缓慢增加。
2.4 等温吸附
在pH 值为4、吸附时间为240min、温度分别取为30℃、35℃和40℃,改变Cr(VI)溶液的初始浓度(10 ~100mg/L),测得改性壳聚糖对Cr(VI)的平衡吸附量与平衡浓度的关系(等温吸附曲线),如图12 所示。

图12 改性壳聚糖对Cr(VI)的等温吸附曲线
常用的等温吸附模型有Langmuir 模型和Freundlich 模型,其线性表达式分别为[21]


式中:q0为改性壳聚糖的饱和吸附量,mg/g;
b为吸附常数,L/mg;
KF和n为常数。
对不同温度下的等温吸附数据分别采用式(3)和式(4)进行拟合,拟合参数如表1所示。

表1 Langmuir 和Freundlich 模型拟合参数
由表1可知,两种等温模型在30℃、35℃、40℃下的线性相关性均较好,R2均大于0.98。
这表明改性壳聚糖对Cr(VI)的吸附同时符合Langmuir模型和Freundlich 模型,其中Langmuir 模型的线性相关性(R2均大于0.99)略优于Freundlich 模型。改性壳聚糖在40℃下,对Cr(VI)的饱和吸附量可达到93.46mg/g。
将本文制备的Fe3O4改性壳聚糖与其他改性壳聚糖的吸附性能进行对比,如表2所示。
由表2可知,Fe3O4改性壳聚糖不仅制备工艺简单,吸附性能也优良。
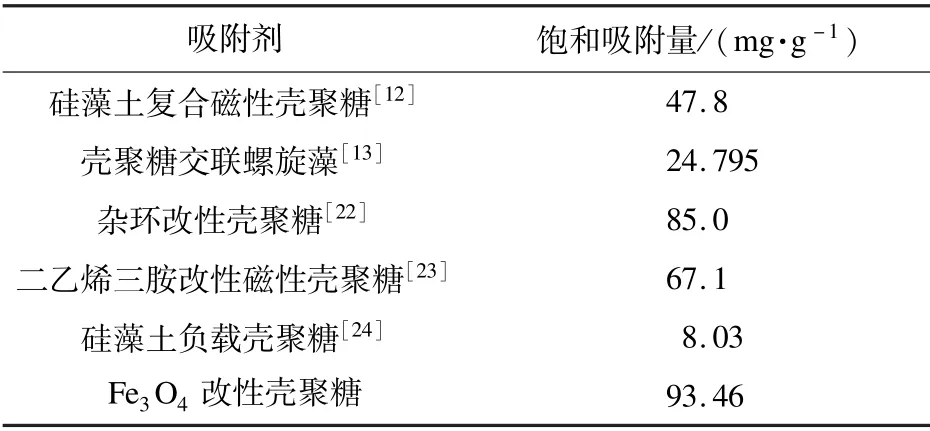
表2 不同吸附剂对Cr(VI)的吸附性能对比
2.5 吸附热力学研究
根据30℃、35℃和40℃下等温吸附数据,对吸附热力学有关参数进行计算,相关公式如下[25-26]。
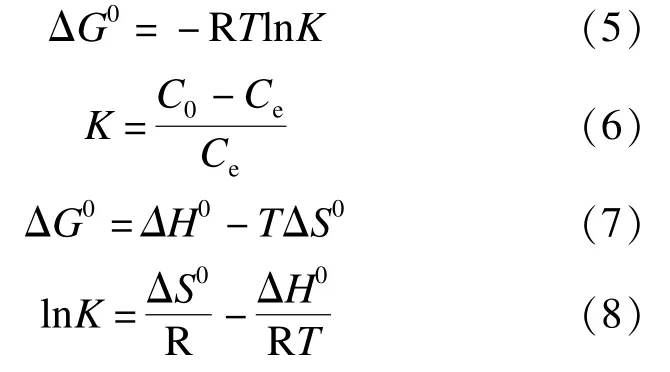
式中:ΔG0为吉布斯自由能,J/mol;
R 为气体常数;
K为分配系数;
ΔH0为焓变,J/mol;
ΔS0为熵变,J/(mol·K);
T为绝对温度,K。
根据式(5) ~式(8)计算ΔS0、ΔH0和ΔG0,结果如表3所示。

表3 吸附热力学相关参数
由表3可以看出,在30℃、35℃、40℃下,改性壳聚糖对Cr(VI)吸附过程的ΔG0值均小于0,且温度升高,ΔG0值减小,表明该吸附为自发过程,且温度越高,自发反应越强。
ΔS0大于0,表明吸附为熵增过程,ΔH0大于0,表明改性壳聚糖吸附Cr(VI)为吸热过程。
(1)采用超声协同化学交联法制备了Fe3O4改性壳聚糖,其表征结果显示Fe3O4成功负载到壳聚糖上,改性壳聚糖表面褶皱、粗糙,布满Fe3O4颗粒。
(2)确定了适宜的改性条件为:Fe3O4投加量0.25g/g,戊二醛用量25mL/g,超声破碎时间5min。在溶液pH 值为4、吸附温度为30℃、吸附时间为240min 时,改性壳聚糖对Cr(VI)的吸附效果较佳,去除率达到57.37%。
(3)改性壳聚糖对Cr(VI)离子的吸附行为符合Langmuir 和Freundlich 等温吸附模型。
吸附热力学计算结果表明Fe3O4改性壳聚糖对Cr(VI)离子的吸附为自发吸热过程。
猜你喜欢 戊二醛谱线壳聚糖 戊二醛添加顺序对胶原蛋白肠衣膜品质的影响食品与生物技术学报(2022年12期)2023-01-10“羲和号”首次获得三种太阳谱线轮廓中国科技财富(2022年8期)2022-12-18氧化石墨烯-壳聚糖复合材料对水体中农药的吸附河北科技师范学院学报(2022年2期)2022-08-26依据不同波段光谱诊断闪电回击通道温度*物理学报(2022年10期)2022-06-04蛇天津诗人(2021年1期)2021-11-12高效液相色谱法测定猪心脏瓣膜假体中戊二醛残留量现代仪器与医疗(2021年2期)2021-07-21三种不同分子量6-羧基壳聚糖的制备、表征及其溶解性河北科技师范学院学报(2021年1期)2021-05-10基于彩色CCD的棱镜摄谱实验数据处理物理实验(2020年12期)2021-01-06戊二醛癸甲溴铵溶液开口稳定性试验研究北方牧业(2019年22期)2019-12-27美洲大蠊药渣制备壳聚糖工艺的优化中成药(2017年12期)2018-01-19本文来源:http://www.zhangdahai.com/shiyongfanwen/qitafanwen/2023/0715/625730.html