【www.zhangdahai.com--其他范文】
尹伶灵,杨志昆,周 晶,商 菲,张含侠,章安源,门晓冬,李有志,田成国,陈 玲*
(1.山东省饲料兽药质量检验中心(山东省畜产品质量安全监测与风险评估重点实验室),济南 250100;
2.青岛欧博方医药科技有限公司,山东青岛 266114;
3.邹平市农业农村局,山东滨州 256200)
兽药复方酮康唑软膏用于治疗犬猫真菌病、厌氧菌等引起的细菌性皮肤病[1]。以酮康唑、甲硝唑为主药,加入薄荷脑、助悬剂,抗氧化剂等制成。现有检测方法收录在《兽药质量标准(2017版)》化学药品卷,酮康唑和甲硝唑的含量是通过分别提取后,采用紫外-可见分光光度法分别测定。该方法需要分别提取,且提取方法复杂,尤其是酮康唑的测定方法,需要先用0.1 mol/L盐酸溶液提取3次,再用三氯甲烷萃取3次,操作繁琐,耗时久,且有机溶媒使用量大(一次检验需易制毒试剂三氯甲烷300多毫升)。中国药典抗真菌感染药复方酮康唑乳膏中酮康唑的含量测定采用液相色谱法[2-3],但其处方中不含甲硝唑。陆国庆等[4]曾尝试用高效液相色谱法等度洗脱同时检测酮康唑乳膏中酮康唑与甲硝唑的含量,但甲硝唑出峰时间太早,不能与溶剂峰能很好地基线分离,且制剂处方相差较大。本试验拟采用反相高效液相色谱梯度洗脱方式,同时测定兽药复方酮康唑软膏制剂中酮康唑和甲硝唑2种药效成分的含量,旨在为兽药复方酮康唑软膏的质量控制提供技术支撑。
1.1 仪器 BT125D 型电子天平(梅特勒-托利多仪器有限公司);
Agilent 1260 型高效液相色谱仪配带二极管阵列检测器(美国 Agilent 公司)。
1.2 药品与试剂 酮康唑对照品 (批号:100294-201904,含量99.8%)、甲硝唑对照品(批号:100191-200305,含量99.6%),均购自中国食品药品检定研究院;
甲醇、乙醇均为色谱纯,德国默克公司生产;
水为符合 GB/T 6682 标准的超纯水。
复方酮康唑软膏(批号:20210110)及软膏空白基质均由青岛欧博方医药科技有限公司提供。
1.3 色谱条件 色谱柱为Agilent Eclipse XDB C18柱(4.6×150 mm,5 μm),柱温:30 ℃,流速:1.0 mL/min;
检测波长:239 nm;
进样体积:10 uL,流动相为甲醇-水,梯度洗脱程序见表1。

表1 液相色谱梯度洗脱程序Tab 1 HPLC gradient elution program
1.4 溶液的制备
1.4.1 对照品溶液的制备 酮康唑对照品溶液:称取酮康唑对照品约16 mg,精密称定,置10 mL量瓶中,加无水乙醇溶解并稀释至刻度,摇匀即得。
甲硝唑对照品溶液:称取甲硝唑对照品约32 mg,精密称定,置10 mL量瓶中,加无水乙醇溶解并稀释至刻度,摇匀即得。
混合对照品溶液:分别精密量取甲硝唑对照品溶液、酮康唑对照品溶液各1 mL,置同一10 mL量瓶中,加溶剂(初始比例流动相)稀释至刻度,摇匀即得(约含酮康唑0.16 mg/mL,甲硝唑唑0.32 mg/mL)。
1.4.2 供试品溶液的制备 取本品约4 g,精密称定,加无水乙醇20 mL,置80 ℃水浴中加热使样品全部溶解[2,5],转移移至50 mL量瓶中,用适量无水乙醇冲洗烧杯3次,放冷至室温,用无水乙醇稀释至刻度,摇匀。置冰浴中冷却2 h[6-8],过滤,弃去初滤液(约5 mL),取续滤液放置至室温。精密量取续滤液2 mL,置10 mL量瓶中,用溶剂(初始比例流动相)稀释至刻度,摇匀即得供试品溶液。(约含酮康唑0.16 mg/mL;
甲硝唑0.32 mg/mL)。
1.4.3 软膏基质样品溶液的制备 取处方中除去甲硝唑、酮康唑制成的软膏基质样品,按照2.2.2项下方法制备,即得。
2.1 系统适用性试验 分别精密吸取混合对照品溶液、供试品溶液、软膏基质样品溶液各 10 μL,按1.3项下色谱条件进样测定。结果显示,甲硝唑峰和酮康唑峰理论板数均大于4000,甲硝唑与酮康唑的分离度大于25,完全分离,且基质无干扰。对照溶液、供试品溶液及软膏基质样品溶液色谱图见图1。
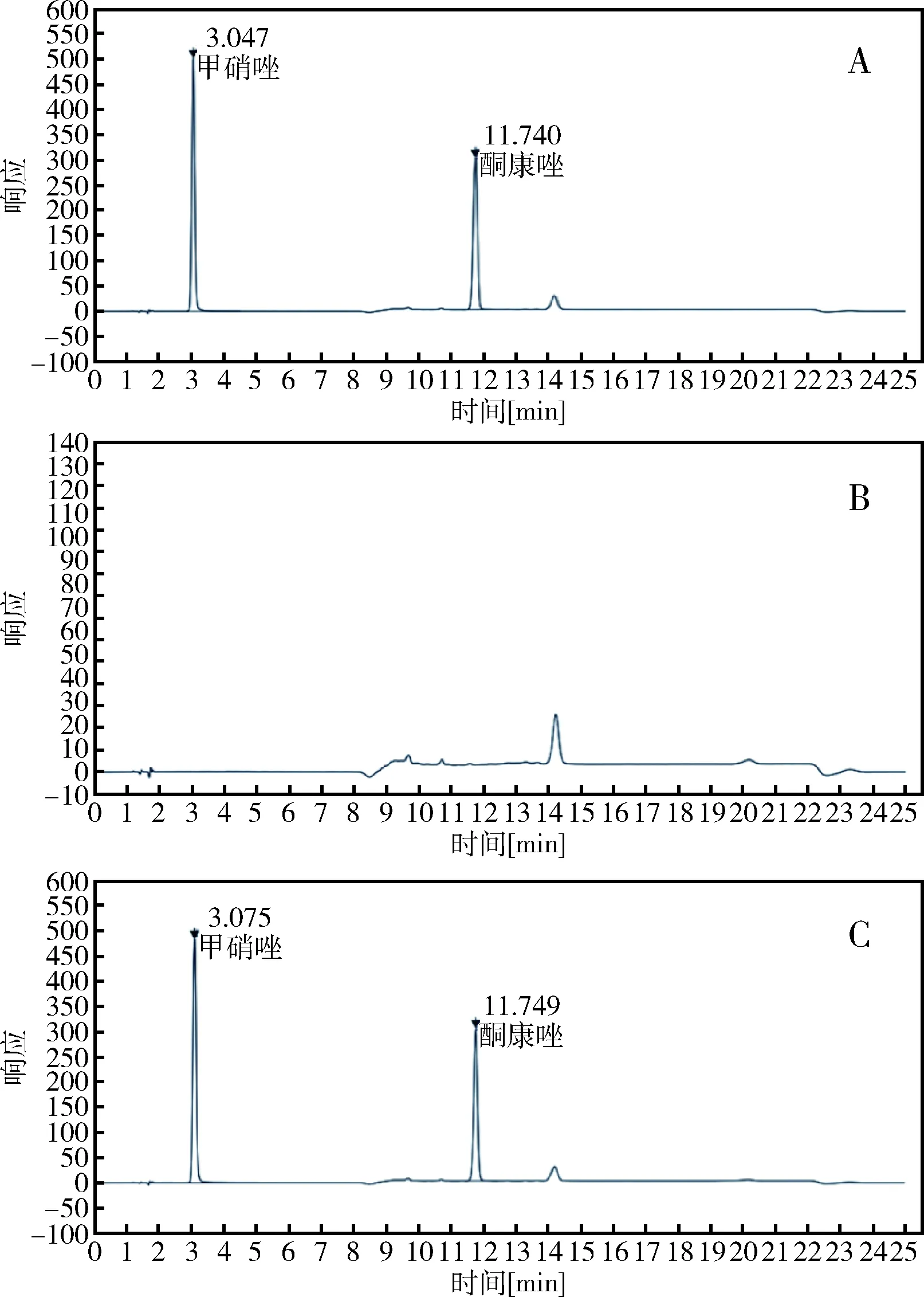
A:甲硝唑、酮康唑混合对照品溶液色谱图;B:软膏基质样品溶液色谱图;
C:供试品溶液色谱图。A:Chromatogram of metronidazole and ketoconazole mixed control substance solution;B:Chromatogram of ointment matrix sample solution;C:Chromatogram of sample solution.图1 HPLC色谱图Fig 1 HPLC Chromatogram
2.2 线性关系试验 将甲硝唑、酮康唑对照品溶液,分别稀释成含甲硝唑0.128、0.192、0.256、0.320、0.384、0.512 mg /mL,含酮康唑0.064、0.096、0.128、0.160、0.192、0.256 mg /mL的混合溶液(标液浓度相当于供试品含量相当于标示量的40%、60%、80%、100%、120%、160%),照1.3项 下色谱条件进样10 μL,记录色谱图。以峰面积为纵坐标(Y),浓度为横坐标(X),绘制标准曲线,甲硝唑的线性回归方程为y=10.014x+40.29,R2=0.9997;
酮康唑的线性回归方程为y=15.337x+40.505,R2=0.9995。表明甲硝唑在0.128~0.512 mg/mL、酮康唑在0.064~0.256 mg/mL 范围内,线性关系良好。
2.3 精密度试验 精密吸取含甲硝唑0.32 mg /mL、酮康唑0.16 mg /mL 的混合对照品溶液,按1.3项下色谱条件进样测定6次,记录色谱图。结果表明,甲硝唑峰面积的RSD为0.2%,酮康唑峰面积RSD为0.3%,证明本方法精密度良好。
2.4 溶液稳定性实验 取供试品溶液室温放置,分别于0、4、8、12、18、24、36、48 h,进样测定,考察供试品溶液的稳定性。48 h内两组分含量的RSD分别为0.99%、0.94%,结果表明供试品溶液在48 h内稳定。
2.5 重复性试验 精密称定复方酮康唑软膏样品(批号:20210110,实际投料量为标示量的100%) 6 份,每份约4 g,按照 1.4.2项下的方法制成供试品溶液,按1.3项下色谱条件进样测定,记录色谱图,以峰面积计算供试品中甲硝唑、酮康唑的含量,结果见表2,表明本方法重复性良好。
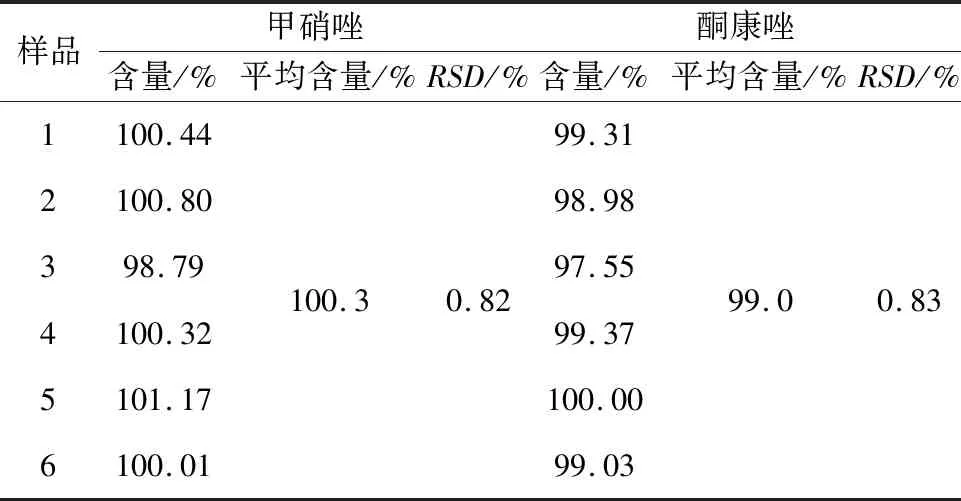
表2 重复性试验结果(n=6)Tab 2 Results of repeated trials (n = 6)
2.6 加样回收率试验 称取软膏基质样品共 9 份,每份约4 g,精密加入含量相当于标示量80%、100%、120%的对照品溶液,按照1.4.2项下的方法制成供试品溶液,按 1.3项下色谱条件进样测定,记录色谱图,以峰面积计算基质添加样品中甲硝唑、酮康唑的含量,计算回收率。甲硝唑平均回收率为100.0%,RSD为0.85%,酮康唑平均回收率为97.8%,RSD为1.28% (n=9)(表3)。

表3 加样回收试验结果及RSD(n=9)Tab 3 The results of recovery test and RSD(n=9)
2.7 实际样品含量测定 取3批不同厂家的已经检验合格的报批检验样品进行复检,按照 1.4.2项下的方法制成供试品溶液,按1.3项下色谱条件进样测定,记录色谱图,以峰面积计算供试品中甲硝唑、酮康唑的含量。结果表明,甲硝唑、酮康唑含量测定结果与《兽药质量标准(2017版)》检测结果相一致,进一步证明了该方法的准确性(表4)。

表4 不同生产厂家样品含量测定结果Tab 4 Determination results of samples from different manufacturers
3.1 色谱条件的选择 对于检测波长的选择,用乙醇做溶剂时,甲硝唑和酮康唑两种组分的紫外吸收图谱见图2。通过二极管阵列检测器,全波长扫描采集图谱后,提取色谱图,最终确定采集波长为239 nm,由图2可以看出在该波长下甲硝唑和酮康唑均有一定的紫外吸收。二极管阵列检测器中峰纯度检测表明,甲硝唑峰和酮康唑峰峰纯度均在995以上,证明该波长和色谱条件下辅料不干扰主成分检测。复方酮康唑软膏中含有较复杂的基质,且不同生产厂家的基质组成不同,因此在供试品测定过程中应避免空白基质峰对样品峰的影响。流动相选择的过程中,通过参考文献[2,9],最终选择甲醇-水体系,梯度洗脱方式,甲硝唑和酮康唑实现了很好的分离,且基质无干扰。与陆国庆等[4]所采用的等度洗脱方式相比,该方法专属性更好,因甲硝唑和酮康唑极性差别大,在液相色谱柱上的保留差别比较大,不适合等度条件下检测。
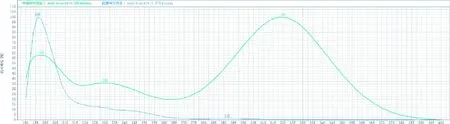
图2 甲硝唑、酮康唑紫外光谱叠加图谱Fig 2 Overlay ultraviolet spectrum of metronidazole and ketoconazole
3.2 提取溶剂的选择 考虑到软膏的油性基质[10-11],为了提高甲硝唑、酮康唑两种主成分的提取效率,参考文献[2,5],本实验选择了对软膏基质和甲硝唑、酮康唑均有一定溶解性,且对操作人和环境友好的乙醇作为提取溶剂。通过对提取溶剂体积、加热温度和时间以及冷却时间的考察,最终确定样品置 80 ℃ 水浴中加热 5 min,振摇,能够使基质全部溶散,甲硝唑、酮康唑提取完全。冰浴冷却又可以使基质冷凝沉淀去除干扰,让测定的专属性更强。
本文建立了同时测定兽药复方酮康唑软膏中酮康唑、甲硝唑含量的高效液相色谱(HPLC)法,采用C18色谱柱,甲醇-水为流动相梯度洗脱,检测波长239 nm。该方法与原标准方法相比,显著缩短了检验周期,减少了有机溶媒的使用,且操作简单,分离度好,准确性高,重现性好,为该制剂的质量控制提供了技术支撑。
猜你喜欢 甲硝唑软膏供试 霍山石斛黄酮组分的UPLC 指纹图谱建立及条件优化农产品加工(2022年7期)2022-05-26克拉霉素联合甲硝唑治疗小儿HP相关性胃炎的临床研究中国药学药品知识仓库(2022年9期)2022-05-23甲硝唑配合红外光治疗慢性宫颈炎的有效性及对复发率的影响中国典型病例大全(2022年7期)2022-04-22小麦全程绿色防控用药试验分析河南农业·综合版(2022年2期)2022-03-18小麦全程绿色防控用药试验分析河南农业(2022年2期)2022-03-14小麦全程防控应用拜耳公司农药产品试验河南农业·综合版(2021年7期)2021-08-23软膏开封别久放百姓生活(2021年2期)2021-05-06软膏开封能放多久恋爱婚姻家庭·养生版(2020年7期)2020-08-10软膏开封能放多久恋爱婚姻家庭(2020年21期)2020-07-23临床一得录祝您健康(1984年6期)1984-12-30本文来源:http://www.zhangdahai.com/shiyongfanwen/qitafanwen/2023/0426/589613.html